拟议机制是什么意思?化学实验中的反应机制如何确定?
新闻图片
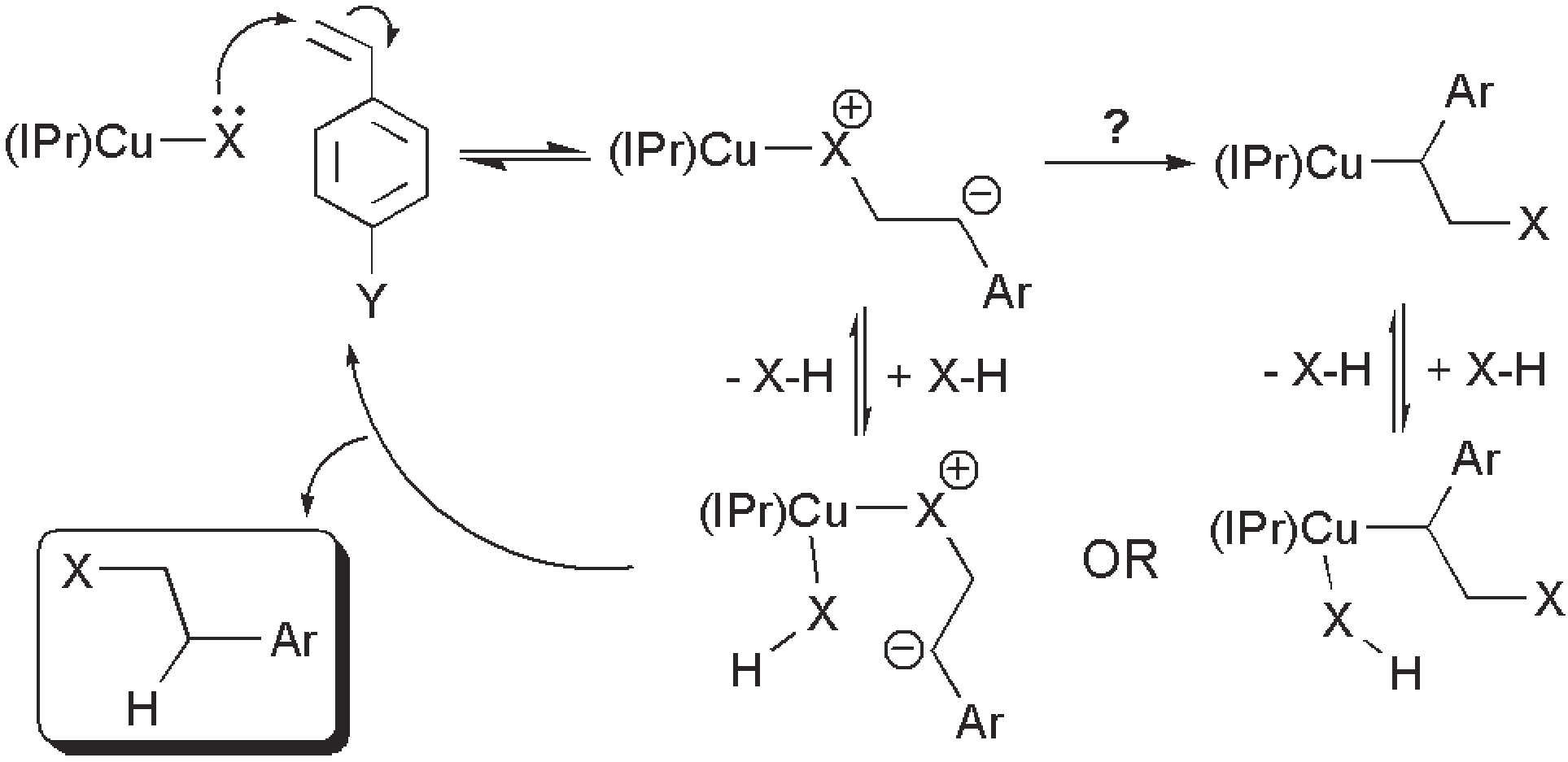
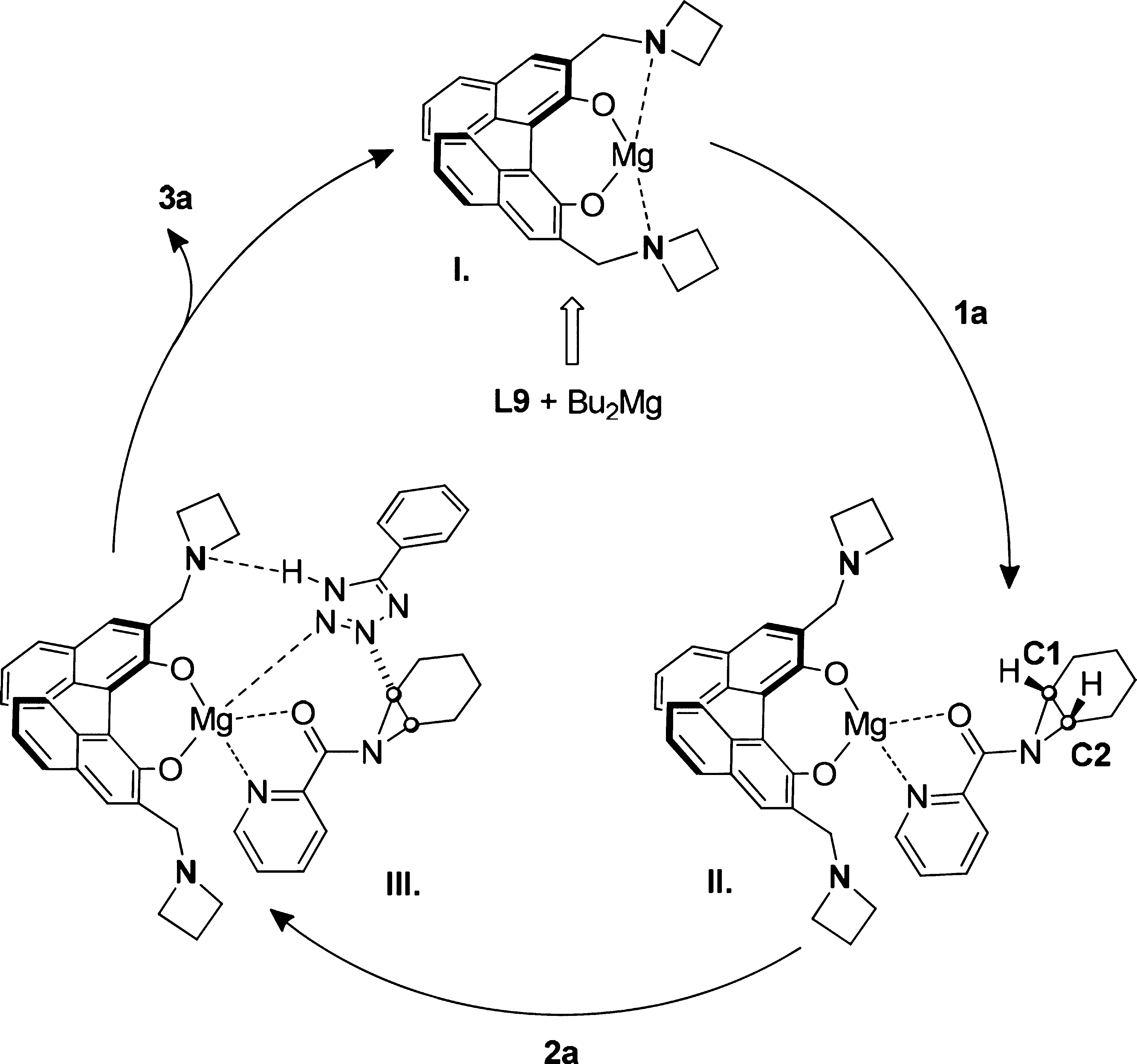
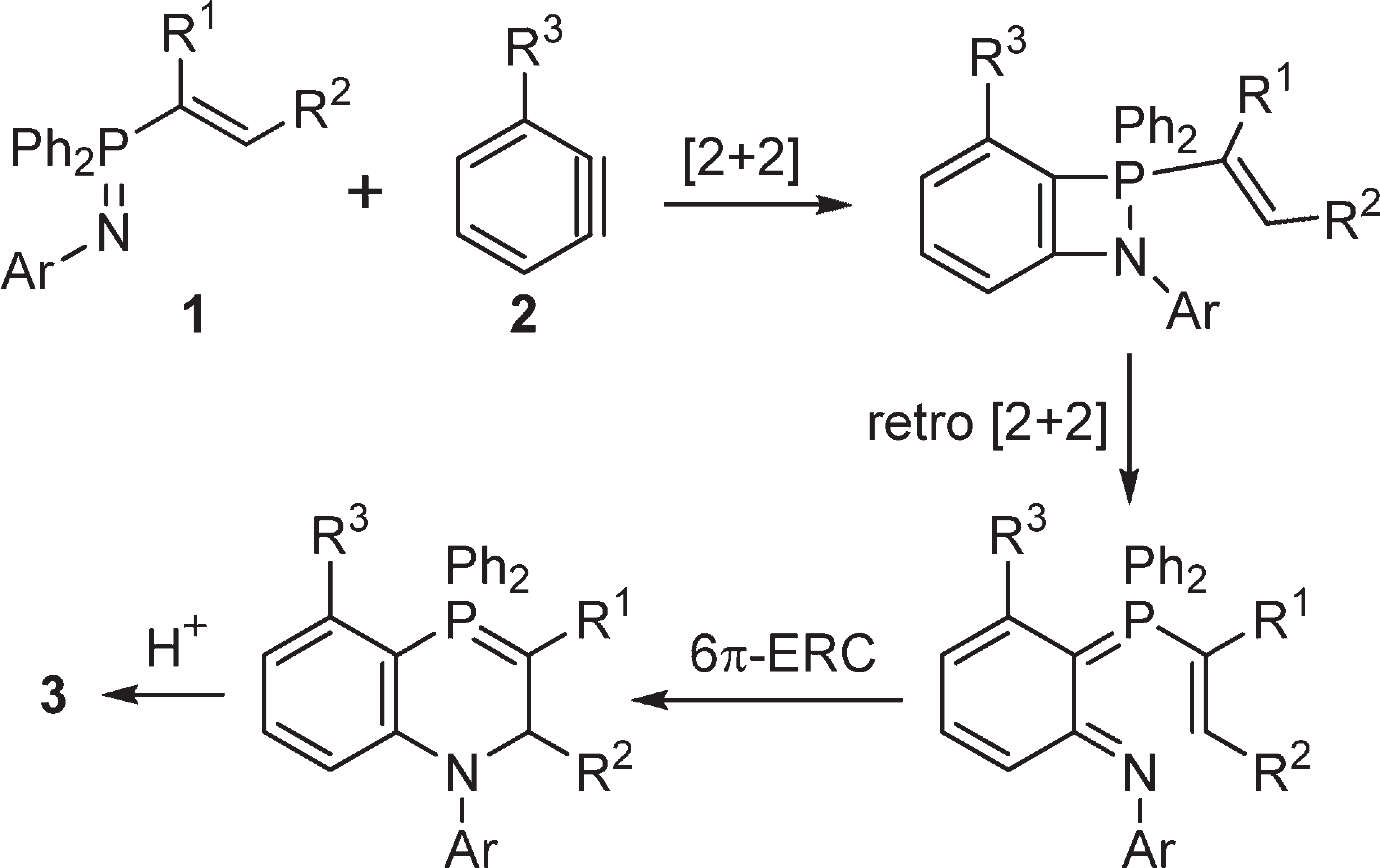
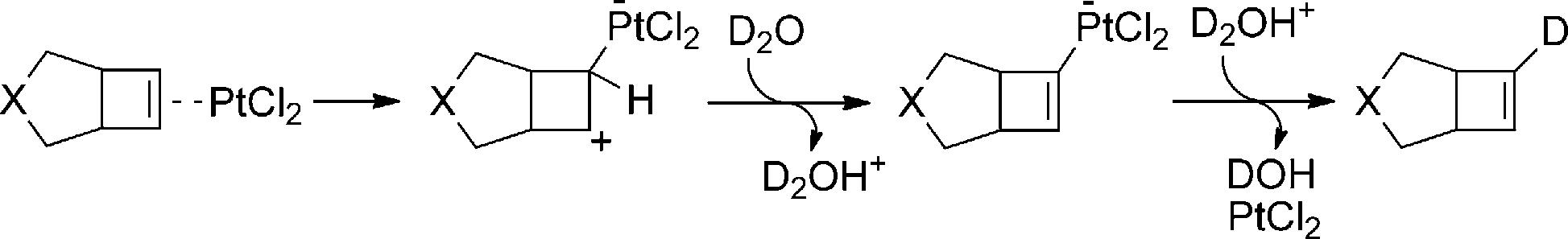
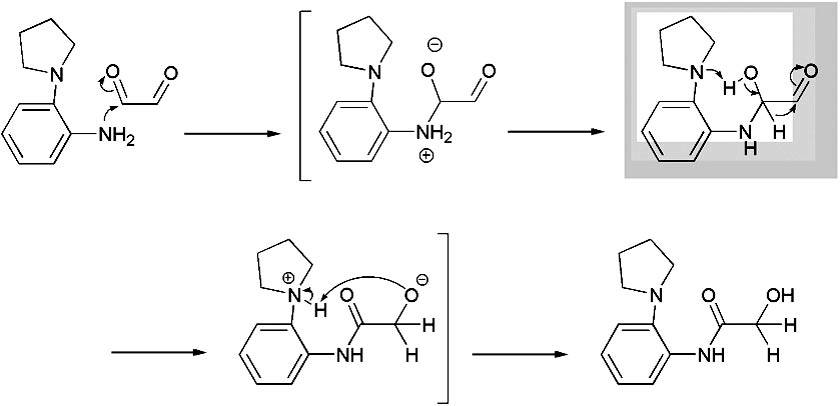
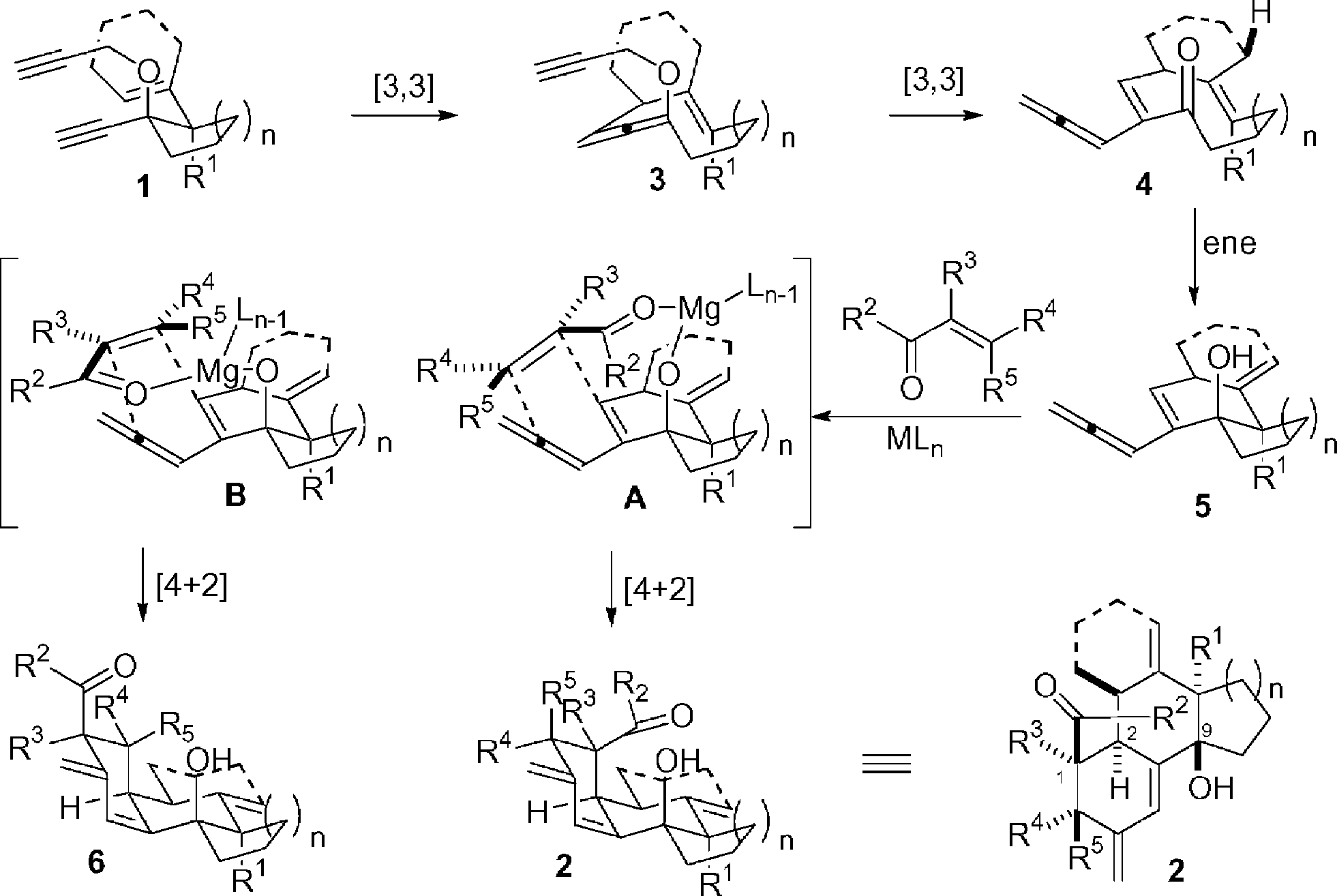
拟议机制并不是一个只存在于化学领域的词汇,广义上指在决策或政策制定过程中,通过提出初步方案、广泛讨论并优化调整的系统性流程。在化学领域要理解拟议机制就必须弄清楚化学实验中的反应机制是如何确定的?
化学实验中的反应机制如何确定?
在化学实验中,确定反应机制是一个系统且复杂的过程,需要综合运用多种实验方法和理论计算手段,以下是根据上述材料对反应机制确定方法的总结:
实验方法
-
动力学研究:
-
速率定律确定:通过测量反应速率与反应物浓度的关系,确定反应的总级数以及各反应物的分反应级数。例如,若反应速率与底物浓度成一级关系,与亲核试剂浓度成零级关系,则支持SN1机理;若反应速率与底物和亲核试剂浓度均成一级关系,则支持SN2机理。
-
速率控制步骤判断:将实验得到的速率定律与所提出的反应机理预测的速率定律进行比较,从而确定反应的速率控制步骤。
-
-
中间体的检测:
-
利用光谱技术:采用核磁共振、红外、紫外 - 可见、电子自旋共振、质谱等光谱技术来检测反应过程中短寿命的中间体。例如,在烯烃的亲电加成反应中,可通过低温下进行反应并利用核磁共振技术检测碳正离子中间体,若检测到碳正离子的存在,则支持该反应存在碳正离子中间体这一步骤。
-
加入捕获剂:对于一些难以直接检测的中间体,可以加入特定的捕获剂与之反应,通过分析产物来间接证明中间体的存在。
-
-
同位素标记实验:
-
追踪原子去向:用稳定的同位素(如H→D、O - 16→O - 18)替换反应物中的特定原子,然后通过分析产物中同位素的分布情况,来追踪原子在反应过程中的去向,从而确定反应机制。例如,在研究乙酸乙酯的水解反应时,将乙酸乙酯中的甲基上的氢原子用氘进行标记,通过分析水解产物中氘的分布,确定是醇中的氢氧键断裂还是酯中的碳氧键断裂。
-
利用动力学同位素效应:如果在反应的限速步骤中涉及氢键断裂,用氘(D)替换氢(H)会使反应速度显著减慢,通过观察反应速率的变化来判断反应机理。
-
-
立体化学证据:产物的空间排列可以为反应机理提供重要线索。例如,对于SN2反应,产物会发生构型反转(背面攻击);对于SN1反应,会发生外消旋化(从平面碳正离子的两侧攻击)。
-
反应条件的影响:研究溶剂、温度、催化剂或添加剂等反应条件对反应的影响,有助于确定反应机理。例如,极性质子溶剂能够稳定碳正离子,从而有利于SN1反应的发生。
理论计算方法
-
量子化学计算:
-
绘制能量分布图:利用量子化学计算软件(如Gaussian等),对反应物、中间体和过渡态的结构和能量进行计算,绘制反应路径上的能量变化图,从而确定反应的活化能和反应热。
-
预测过渡态、中间体和活化能:通过计算预测反应过程中的过渡态结构、中间体的稳定性以及活化能等,并将这些理论计算结果与实验数据进行比较,以验证反应机理的合理性。例如,在研究一个有机分子的重排反应时,通过量子化学计算找到反应路径上的过渡态结构,若计算出的过渡态能量较低,且与实验测得的反应活化能相符,则可确定这个过渡态是反应机制中的关键步骤。
-
-
分子动力学模拟:研究反应体系在一定时间内的运动过程,了解反应物分子之间的碰撞、能量传递等微观过程。例如,在研究气体相反应时,通过分子动力学模拟观察分子之间的碰撞角度、碰撞能量等因素对反应发生的影响,将模拟结果与实验中控制的反应条件进行对比,从而确定反应机制中分子碰撞的特征。
确定反应机制的过程
-
提出“拟议机制”:当化学家观察到一个新反应时,首先会根据已有的化学知识(如电子效应、空间效应、已知的经典机制等)来推测反应可能的发生方式,提出一个或多个“拟议机制”,作为工作的假设蓝图。拟议机制的作用是提供解释框架,解释初始观察到的现象,如反应条件的要求、主要产物和副产物的生成等;同时,它还能指导实验设计,指明需要寻找哪些证据来证明自己。
-
设计实验检验“拟议机制”:根据拟议机制中的具体预测,设计相应的实验来收集证据。实验方法包括动力学研究、中间体鉴定、同位素标记、立体化学研究、同位素效应以及理论计算等。例如,若拟议机制提议决速步是单分子反应(如SN1),则通过动力学研究测定反应速率与反应物浓度的关系,若实验结果与预测相符,则支持该机制;若拟议机制中有碳正离子中间体,则通过中间体鉴定实验来检测其是否存在。
-
评估与修正“拟议机制”:将实验结果与拟议机制的预测进行比对。如果多个独立的实验证据都支持同一个拟议机制,而没有任何证据与之矛盾,那么这个机制的可信度就非常高,会被科学界暂时接受为“当前最合理的机制”;如果某个关键实验的结果与拟议机制的预测不符,则该拟议机制被证伪,必须被放弃或进行重大修正。
拟议机制是什么意思?
在化学领域,“拟议机制”(Proposed Mechanism) 是指科学家为解释一个化学反应如何从分子层面发生而提出的、基于实验证据的、逐步的理论模型。它不是对反应结果的简单描述,而是深入揭示反应物转化为产物的详细路径,包括中间步骤、键的变化、能量变化以及催化剂的作用等。
简而言之,拟议机制是化学反应的“分子级故事”。
一、拟议机制的核心内容
一个完整的拟议机制通常包含以下关键要素:
-
反应步骤的分解
反应是否一步完成?还是经过多个中间步骤?例如,SN1反应分为“碳正离子生成”和“亲核进攻”两步。 -
中间体的识别
是否生成了短暂存在的中间体?如碳正离子、自由基、碳负离子、环状溴鎓离子等。这些中间体是机制推理的关键。 -
键的断裂与形成方式
化学键是均裂(产生自由基)还是异裂(产生离子)?键的断裂与形成是同步还是分步进行? -
过渡态与能量变化
每一步反应的高能过渡态是什么?哪一步能量最高(即速率决定步骤)? -
催化剂与溶剂的作用
催化剂如何参与反应?是先吸附反应物(如L-H机制),还是直接与气相分子反应(如E-R机制)?酶如何通过“诱导契合”降低活化能? -
立体化学结果的解释
为什么产物具有特定的立体构型?例如,反式加成支持溴鎓离子机制,而非碳正离子机制。
二、为什么需要“拟议”机制?
提出机制的目的远不止“解释一个反应”,它具有深远的科学与应用价值:
-
解释实验现象:
为什么反应速率只与一种反应物浓度有关?为什么需要特定溶剂或温度?机制能给出根本原因。 -
预测反应行为:
一旦理解机制,就能预测类似结构的分子在相同条件下的反应路径和产物。 -
优化反应条件:
通过识别速率决定步骤,可针对性地改进催化剂、溶剂或温度以提高产率。 -
设计新反应:
机理知识是合成新药物、新材料的基础。例如,基于过渡态理论设计酶抑制剂。
三、如何“拟议”并验证一个机制?——科学探究的循环
“拟议”不是凭空猜测,而是一个严谨的科学过程:
1. 收集实验证据
-
动力学研究:测定速率定律。
例:叔丁基溴水解速率只与[(CH₃)₃C-Br]有关 → 支持SN1机制(决速步为单分子解离)。 -
中间体的检测:
- 光谱法(NMR、IR)捕捉瞬态物种。
- 低温分离或化学捕获中间体。
-
同位素标记:追踪原子去向。
例:用¹⁸O标记水进行酯水解,发现¹⁸O进入羧酸 → 证明为酰氧键断裂机制。 -
立体化学分析:
例:烯烃加溴得外消旋体 → 支持反式加成的溴鎓离子机制。 -
催化剂研究:改变催化剂结构,观察活性变化,推断其作用方式(如L-H vs E-R机制)。
2. 提出机制
整合所有证据,构建一个自洽的、逐步的反应路径图,能够解释所有观察到的现象。
3. 验证与修正
- 理论计算:使用DFT等方法计算各步能量,验证过渡态和中间体的稳定性。
- 设计验证实验:根据机制预测新条件下的结果,并实验检验。若不符,则修正机制。
四、经典案例:叔丁基溴的碱性水解
- 总反应:(CH₃)₃C-Br + OH⁻ → (CH₃)₃C-OH + Br⁻
- 实验现象:速率 = k [(CH₃)₃C-Br],与[OH⁻]无关
- 拟议机制:SN1机制
- (CH₃)₃C-Br → (CH₃)₃C⁺ + Br⁻(慢,决速步)
- (CH₃)₃C⁺ + OH⁻ → (CH₃)₃C-OH(快)
- 解释:决速步不涉及OH⁻,故其浓度不影响速率。
五、重要提醒:机制是“模型”,而非“真理”
- 拟议机制是当前证据下最合理的解释,但不是最终定论。
- 随着新工具(如超快光谱、高精度计算)的发展,旧机制可能被修正或推翻。
- 科学进步正是通过“提出机制 → 实验验证 → 修正模型”的循环实现的。